
骨关节炎(OA)是一种极为常见的退行性关节疾病,主要表现为关节软骨的磨损和流失。在所有受影响的人群中,女性尤其是绝经后的女性发病率明显高于男性。
近年来,再生医学界将目光投向了“间充质基质细胞(MSCs)”。这类细胞分泌的“细胞外囊泡(EVs)”携带了丰富的蛋白质、脂质和核酸,能够充当细胞间的通讯信使,被认为是极具潜力的“无细胞疗法”。
传统的囊泡多提取自骨髓或脂肪组织,但《Scientific Reports》最新发表的一项研究:经血来源的间充质基质细胞(MenSCs)。这些细胞可通过完全无创的方式定期获取,且被证明同样拥有强大的修复能力。

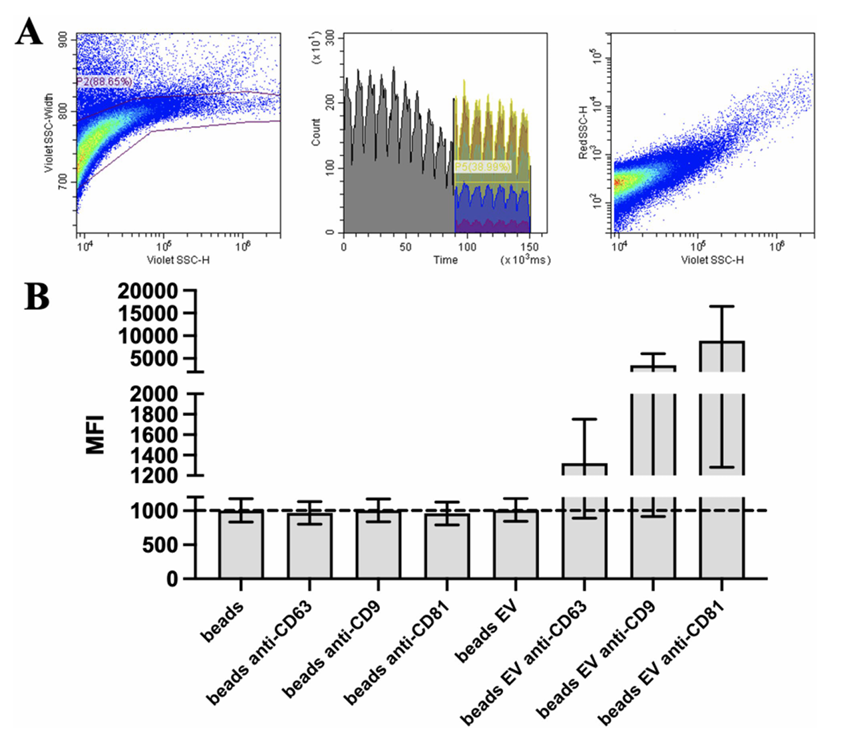
研究团队首先从健康女性的经血中分离出间充质基质细胞,并利用分子排阻色谱法提取了其中的细胞外囊泡(MenSC-EVs)。通过流式细胞术检测,确认这些囊泡不仅尺寸符合标准(80-300纳米),并且表面带有经典的标志物蛋白CD63、CD81和CD9。
要让囊泡发挥作用,首先得确保它们能被关节软骨细胞吸收。实验显示,经过荧光标记的囊泡在短短3小时内就被人类软骨细胞高效摄取。在显微镜下连续追踪细胞轨迹发现,囊泡的处理并没有改变软骨细胞的自然迁移能力、运动速度、细胞周长以及长期的增殖活性。这说明MenSC-EVs在提供修复信号的同时,具备极高的生物相容性,不会对正常细胞的生理节奏造成干扰。
女性绝经后雌激素和孕激素水平的断崖式下降,是骨关节炎高发的核心原因之一。软骨细胞表面含有这两种性激素的受体,它们在维持软骨基质的合成中起着支撑作用。
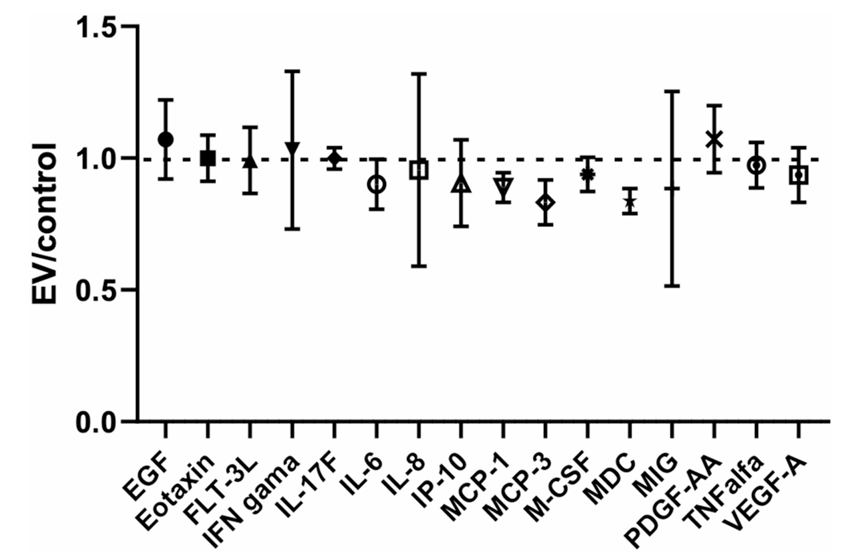
研究人员在单层软骨细胞培养中发现,使用MenSC-EVs处理后,软骨细胞内部的孕激素受体(PGR)在蛋白层面和基因层面均出现了显著的表达增加,而雌激素受体(ESR1)则保持稳定。鉴于孕激素在促进软骨细胞存活和基质稳态中的作用,这种特异性上调受体的能力,揭示了经血来源囊泡在治疗女性专属骨关节炎中的独特潜力。同时,对分泌物的多重因子分析显示,囊泡处理并未引发炎症细胞因子的异常分泌,维持了稳定的软骨免疫微环境。
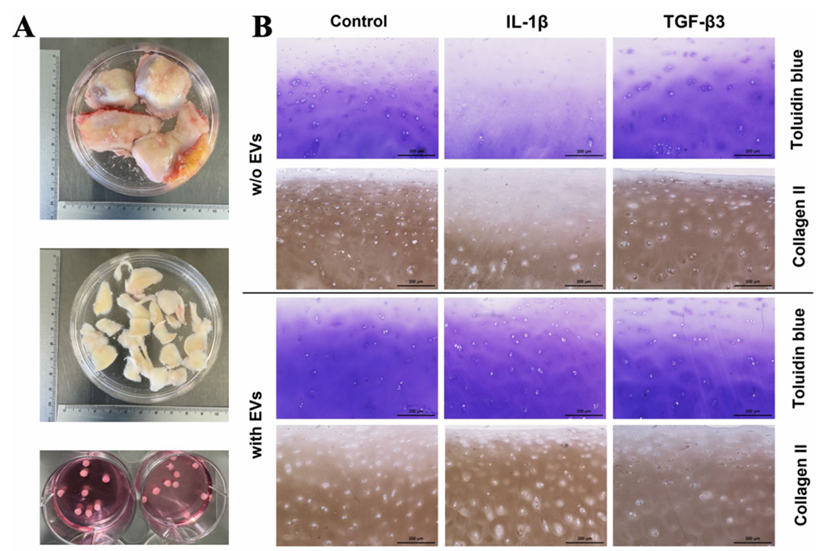
为了更贴近人体内的真实情况,研究利用软骨细胞培养了3D微球模型,并在培养液中加入了促成骨/软骨分化的生长因子TGF-β3。组织学染色(番红O和甲苯胺蓝)直观地显示,联合使用囊泡和TGF-β3,使得微球中合成了更为浓密的细胞外基质(ECM)。
基因层面的数据进一步支撑了这一结果:囊泡的加入不仅显著增强了II型胶原(软骨的核心结构蛋白)的基因(COL2A1)表达,还大幅上调了TGF-β3受体(TGFBR2)的表达。这意味着囊泡让软骨细胞对生长因子的吸收更加敏感,放大了自身的修复能力。
如果说3D微球验证了“促生”能力,那么直接使用人体关节软骨外植体(真实的软骨组织块),则是为了检验囊泡“抗破坏”的实力。研究人员使用炎性因子IL-1β来模拟关节炎发作时恶劣的内部环境。
在IL-1β的攻击下,软骨外植体会发生明显的降解。然而,在加入了MenSC-EVs的实验组中,组织切片染色显示基质的流失得到了有效遏制,软骨内部的胶原网络得以更好地保存。
软骨一旦被破坏,内部的糖胺聚糖(GAG)和软骨寡聚基质蛋白(COMP)就会像漏水的海绵一样释放到周围环境中。检测证实,无论是在修复环境还是在IL-1β制造的炎症环境下,囊泡的处理都显著减少了GAG和COMP这两种降解标志物的释放。在这场保卫战中,囊泡依然保持了优良的免疫调节特性,除了轻微的IL-6波动外,并没有激起强烈的促炎反应。
未来前景
这项研究清晰地勾勒出了经血来源间充质细胞外囊泡的工作逻辑:它们能够安全地穿透软骨细胞,通过上调关键激素受体、促进胶原和蛋白聚糖的基因表达,不仅能在健康状态下加速软骨基质的合成,更能在炎症侵袭时为软骨组织提供坚实的保护伞。
相较于传统的干细胞移植,这种基于囊泡的“无细胞疗法”免疫原性更低、引发血管栓塞或排异反应的风险更小。而经血这一取之不尽的非侵入性来源中国股票配资官网,更赋予了其极高的伦理和临床可行性。尤其针对绝经后高发关节炎的女性群体,这种疗法或许将在未来的骨科再生医学中占据重要的一席之地。
爱配资提示:文章来自网络,不代表本站观点。
- 上一篇:今日低价股票排名 哈啰单车,被约谈
- 下一篇:没有了



